Pembuktian bahwa atom bukan merupakan bagian terkecil dari suatu zat atau materi ditandai dengan ditemukannya elektron oleh Sir John Joseph Thomson. Pembuktian ini semakin menguat ketika imuwan berkebangsaan inggris ,Ernest Rutherford berhasil menemukan bahwa inti atom masih tersusun dari bagian yang lebih kecil berupa proton dan neutron. Elektron, proton, dan neutron menjadi partikel dasar yang menyusun sebuah atom.
A. Partikel penyusun atom
1.Proton
Eugen Goldstein pada tahun 1886 melakukan perobaan dengan memodifikasi tabung sinar katoda yang ditemukan oleh William Crookes dengan cara melubangi lempeng katoda. Dari percobaan ini ditemukan bahwa gas yang berada di belakang katode menjadi berpijar. Hal ini berarti radiasi dari anode menembus lempengan katode melalui lubang yang sebelumnya telah dibuat.Alhasil,dari percobaan tersebut diketahui ada sebuah sinar yng berlawanan arah dengan sinar anoda. Ia bergerak dari anoda ke katoda.Eugen goldstein menyimpulkan bahwa sinar tersebut meruakan partikel dasar bermuatan positif.

2.Neutron
Setelah ditemukan adanya proton di dalam inti atom, didapati bahwa ternyata massa inti atom selalu lebih besar daripada proton. Darisinilah kemudian para peneliti berpendapat bahwa ada partikel lain di dalam inti (selain proton) yang muatannya netral.
W. Bothe dan H. Becker pada tahun 1930 melakukan penembakan menggunakan partikel alpha (α) ke inti atom berilium. Ditemukan adanya radiasi partikel yang memiliki daya tembus besar. Dua tahun sesudahnya yaitu tahun 1932, James Chadwick melakukan penelitian lebih lanjut dimana ditemukan bahwa partikel tersebut bermuatan netral dan memiliki massa hampir sama dengan partikel proton (bermuatan positif). Partikel ini kemudian dinamakan sebagai neutron.
3.Elektron
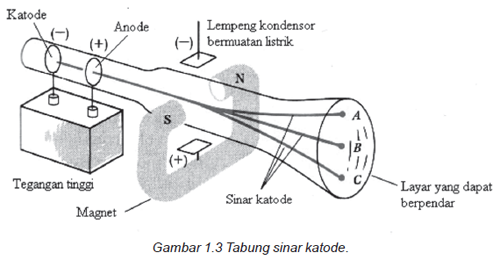
Joseph John Thomson pada tahun 1897 melakukan percobaan dengan menggunakan tabung sinar katode. Terdapat dua plat elektroda dimana salah satu plat logam yang terdapat pada ujung tabung berfungsi sebagai katoda. Kedua plat ini dimasukkan ke dalam tabung kaca bertekanan rendah kemudian dialirkan listrik bertegangan tinggi hingga mampu melepas elektron dari katoda ke anoda. Percobaan ini membuktikan bahwa sinar yang memancar dari plat katoda tersebut merupakan partikel yang lebih kecil dari atom dan ia bermuatan negatif,yang disebut elektron.
B. Bilangan Kuantum
Setiap orbital atom memiliki satu set tiga bilangan kuantum yang unik, antara lain bilangan kuantum utama (n), azimuth (atau momentum angular) (l), dan magnetik (ml).Lalu, terdapat bilangan yang keempat, yakni bilangan kuantum spin (ms), yang memberikan informasi spin suatu elektron dalam sebuah orbital.
1.Bilangan kuantum utama (n)
mendeskripsikan ukuran dan tingkat energi orbital. Semakin besar nilai n, maka semakin besar ukuran orbital dan semakin tinggi tingkat energinya. Nilai n yang diperbolehkan adalah bilangan bulat positif (1, 2, 3, dan seterusnya).
2.Bilangan kuantum azimuth (l)
mendeskripsikan bentuk orbital. Nilai l yang diperbolehkan adalah bilangan bulat dari 0 hingga n − 1.
3.Bilangan kuantum magnetik (ml)
mendeskripsikan orientasi orbital. Nilai ml yang diperbolehkan adalah bilangan bulat dari −l hingga +l
.
.
4.Bilangan kuantum spin (ms)
mendeskripsikan arah spin elektron dalam orbital. Nilai ms yang diperbolehkan adalah +½ atau −½.

Kombinasi bilangan kuantum n, l, dan ml yang mungkin pada 4 kulit elektron pertama dapat dilihat pada tabel berikut
Bentuk Orbital Atom
Orbital s
Orbital s adalah orbital dengan l = 0 berbentuk bola dengan inti atom pada bagian tengah. Oleh karena bola hanya memiliki satu orientasi, semua orbital s hanya memiliki satu nilai ml, yaitu ml = 0. Orbital 1s memiliki densitas (kerapatan) elektron tertinggi pada bagian inti atom dan kemudian densitas semakin menurun perlahan-lahan setelah menjauh dari inti atom. Orbital 2s memiliki dua daerah dengan densitas elektron tinggi. Di antara kedua daerah tersebut terdapat simpul bola, di mana probabilitas menemukan elektron pada daerah tersebut menurun hingga nol (ψ2 = 0). Pada orbital 3s, terdapat tiga daerah dengan densitas elektron tinggi dan dua simpul. Pola bertambahnya simpul orbital s ini masih terus berlanjut dengan orbital 4s, 5s, dan seterusnya
.
.
Orbital p
Orbital dengan l = 1 berbentuk seperti balon terpilin dengan dua cuping. Kedua cuping terletak pada dua sisi inti atom yang saling bersebrangan. Inti atom terletak pada bidang simpul orbital p, yakni di antara dua cuping yang masing-masing memiliki densitas elektron tinggi. Orbital p memiliki tiga jenis orientasi ruang, px, py, dan pz, sebagaimana terdapat tiga nilai ml yang mungkin, yaitu −1, 0, atau +1. Ketiga orbital p tersebut terletak saling tegak lurus pada sumbu x, y, dan z koordinat Kartesius dengan bentuk, ukuran, dan energi yang sama.

Orbital d
Orbital d adalah orbital dengan l = 2. Orbital d memiliki lima jenis orientasi, sebagaimana terdapat lima nilai ml yang mungkin, yaitu −2, −1, 0, +1, atau +2. Empat dari lima orbital d, antara lain dxy, dxz dyz, dan dx2−y2, memiliki empat cuping seperti bentuk daun semanggi. Orbital d kelima, dz2, memiliki dua cuping utama pada sumbu z dan satu bagian berbentuk donat pada bagian tengah

Orbital f
Orbital f adalah orbital dengan l = 3. Orbital f memiliki tujuh jenis orientasi, sebagaimana terdapat tujuh nilai ml yang mungkin (2l + 1 = 7). Ketujuh orbital f memiliki bentuk yang kompleks dengan beberapa cuping.

C. Nomor Atom dan Nomor Massa
1). Nomor Atom
Nomor atom suatu unsur menunjukkan jumlah proton yang terdapat dalam atom. Dalam atom netral jumlah proton sama dengan jumlah elektron, sehingga nomor atom juga menunjukkan banyaknya jumlah elektron yang terdapat pada atom. Hal ini berlaku untuk atom netral. Nomor atom diberi lambang Z.
2). Nomor massa
Nomor massa menggambarkan massa partikel-partikel penyusun atom, yaitu massa proton, massa elektron, dan massa neutron. Massa elektron sangat kecil dibandingkan massa proton dan neutron sehingga massa elektron ini dapat diabaikan. Nomor massa diberi notasi A dan dapat didefenisikan sebagai jumlah proton dan jumlah neutron.
 12 adalah nomor massa dan 6 adalah nomor atom
12 adalah nomor massa dan 6 adalah nomor atom- Jumlah Neutron = Nomor massa – Nomor atom
Jadi jumlah neutron = 12 – 6 = 6 - Jumlah Proton = Nomor atom
Jumlah proton = 6
D. Konfigurasi Elektron
1.Asas Afbau
Elektron menempati orbital-orbital dimulai dari tingkat energi yang terendah, dimulai dari 1s, 2s, 2p, dan seterusnya seperti urutan subkulit

2.Asas larangan Pauli
Tidak ada dua elektron dalam satu atom yang memiliki ke-4 bilangan kuantum yang sama.Setiap orbital maksimum diisi oleh 2 elektron yang memiliki spin yang berlawanan.
3.Kaidah Hund
Jika ada orbital dengan tingkat energi yang sama, konfigurasi elektron dengan energi terendah adalah dengan jumlah elektron tak berpasangan dengan spin paralel yang paling banyak.

DAFTAR PUSTAKA
https://www.studiobelajar.com/konfigurasi-elektron/https://www.studiobelajar.com/konfigurasi-elektron/
https://www.ilmukimia.org/2013/05/bilangan-kuantum.htmlhttps://www.ilmukimia.org/2013/05/bilangan-kuantum.html
Elektron menempati orbital-orbital dimulai dari tingkat energi yang terendah, dimulai dari 1s, 2s, 2p, dan seterusnya seperti urutan subkulit
2.Asas larangan Pauli
Tidak ada dua elektron dalam satu atom yang memiliki ke-4 bilangan kuantum yang sama.Setiap orbital maksimum diisi oleh 2 elektron yang memiliki spin yang berlawanan.
3.Kaidah Hund
Jika ada orbital dengan tingkat energi yang sama, konfigurasi elektron dengan energi terendah adalah dengan jumlah elektron tak berpasangan dengan spin paralel yang paling banyak.
DAFTAR PUSTAKA
https://www.studiobelajar.com/konfigurasi-elektron/https://www.studiobelajar.com/konfigurasi-elektron/
https://www.ilmukimia.org/2013/05/bilangan-kuantum.htmlhttps://www.ilmukimia.org/2013/05/bilangan-kuantum.html
bagusss kak
BalasHapusbagus materinya kak
BalasHapuswah abis baca jadi pinter
BalasHapusTerima kasih, materinya sangat membantu manambah wawasan.
BalasHapusWahh Membantu sekali kak
BalasHapusMakasih kak materinya.sangat bermanfaat
BalasHapuspaten x kaka guaaaa
BalasHapusSa pu pekerjaan rumah,liat dari sini saja to,mantab sudah
BalasHapusMaterinya sangat bermanfaat
BalasHapusMaterinya sangat bermanfaat
BalasHapuskemarin saya belajar diruang makan dan tidak mengerti apa2 tentang atom,namun setelah membaca ini saya tertarik untuk membuat bom atom
BalasHapussemoga dapat nilai yang besar kak
BalasHapusMaterinya sangat bermanfaat kak
BalasHapusSangat membantu saya dalam belajar .terimakasih kak
BalasHapusmembantu sekali kak materinya
BalasHapusKomentar ini telah dihapus oleh pengarang.
HapusMantaps
BalasHapusSyukakk
BalasHapusSangat lengkap kak
BalasHapusKa gracia, perbedaan model atom Bohr dengan model atom Rutherford itu apa?
BalasHapusKalau model atom Rutherford tidak menjelaskan tingkat energi dalam atom,tetapi kalau bhor menjelaskan tingkat energi dalam atom.semoga membantu ya kak☺
HapusTerimakasih saya jadi bisa mengerjakan tugas dari guru saya��
BalasHapusSangat bermanfaat informasinya.. Pengetahuan saya juga bertambah tentang materi ini. Trimakasih..
BalasHapusSangat bermanfaat sekali kak
BalasHapussaya yg jurusan ekonomi rada kurang paham, tp stlh baca blog ini, ya ttp ga paham lah 😂
BalasHapus👍👍👍
BalasHapusNice👍👍👍 ditunggu postingan berikutnya
BalasHapusmantapp
BalasHapusNicw
BalasHapus👍👍👍👍
BalasHapusniceee
BalasHapus👍👍👍
BalasHapusNtaps
BalasHapusGood gracia🐣🐣
BalasHapusGood kakak🙂👌
BalasHapusBaguss
BalasHapusSukak😍
BalasHapusTerima kasih, blognya sangat bermanfaat😊
BalasHapusBagus banget materinya
BalasHapus