Kata asam berasal dari bahasa Latin "acidu” yang berarti masam. Asam adalah zat (senyawa) yang menyebabkan rasa masam pada berbagai materi. Basa adalah zat(senyawa) yang dapat beraksi dengan asam, menghasilkan senyawa yang disebut dengan garam. Sedangkan basa adalah zat yang dapat menetralkan asam. Secara kimia, asam dan basa saling berlawanan. Sifat basa pada umumnya ditunjukkan dari rasa pahit dan licin
. Suatu senyawa disebut asam jika memiliki pH kurang dari 7, dan disebut basa jika memiliki pH lebih dari 7. Asam dapat didefinisikan sebagai zat yang jika dilarutkan dalam air akan mengalami disosiasi dan menghasilkan kation hidrogen (H+), sedangkan basa dapat didefinisikan sebagai zat yang jika dilarutkan dalam air akan mengalami disosiasi dan menghasilkan anion hidroksida (OH-).


2.Teori Bronsted Lowrey yang mengatakan bahwa asam adalah senyawa yang bisa memberi proton (H+) untuk senyawa lain, sedangkan untuk basa bisa menerima proton (H+) pada senyawa lain. Reaksi asam basa dapat mereaksi perpindahan suatu proton pada satu senyawa ke senyawa yang lainnya.

Untuk menyatakan tingkat atau derajat keasaman suatu larutan, pada tahun 1910, seorang ahli dari Denmark, Soren Lautiz Sorensen memperkenalkan suatu bilangan yang sederhana. Bilangan ini diperoleh dari hasil logaritma konsentrasi H+.Bilangan ini kita kenal dengan skala pH. Harga pH berkisar antara 1 – 14 dan ditulis:
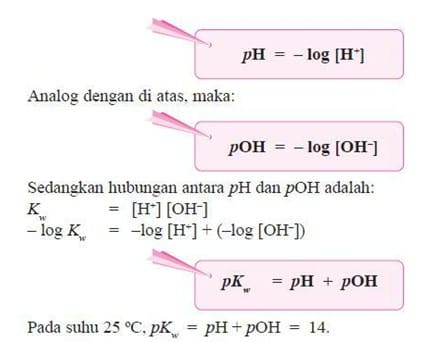
Dapat disimpulkan bahwa :
2.Teori Bronsted Lowrey yang mengatakan bahwa asam adalah senyawa yang bisa memberi proton (H+) untuk senyawa lain, sedangkan untuk basa bisa menerima proton (H+) pada senyawa lain. Reaksi asam basa dapat mereaksi perpindahan suatu proton pada satu senyawa ke senyawa yang lainnya.

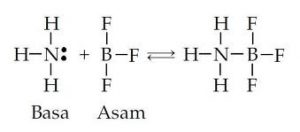
3.Teori Lewwis yang mengatakan bahwa Asam merupakan suatu senyawa yang bisa menerima pasangan elektron bebas pada senyawa lain, sedangkan untuk Basa merupakan suatu senyawa yang bisa memberi pasangan elektron bebas kepada senyawa yang lainnya. Reaksi asam basa merupakan suatu reaksi untuk membentuk ikatan antara asam dan basa.
Indikator asam basa adalah suatu senyawa yang ditambahkan kepada larutan, tujuannya untuk mengetahui kisaran pH pada larutan tersebut.Pada latutan yang akan dilihat tingkat keasamannya akan ditambahkan asam basa yang sesuai. Lalu akan dilakukan titrasi, perubahan pada pH akan diketahui pada perubahan warna larutan yang didalamnya terdapat indikator. Pada perubahan warna sesuai pada kisaran pH dengan indikatornya.
Contoh Daftar Indikator Asam Basa :

B.Indikator Asam Basa
Indikator asam basa adalah suatu senyawa yang ditambahkan kepada larutan, tujuannya untuk mengetahui kisaran pH pada larutan tersebut.Pada latutan yang akan dilihat tingkat keasamannya akan ditambahkan asam basa yang sesuai. Lalu akan dilakukan titrasi, perubahan pada pH akan diketahui pada perubahan warna larutan yang didalamnya terdapat indikator. Pada perubahan warna sesuai pada kisaran pH dengan indikatornya.
Contoh Daftar Indikator Asam Basa :
C.Derajat Kesamaan (pH)

Dapat disimpulkan bahwa :
trima kash kaka👍👍👍
BalasHapusBagussss bangettt kak graciaa, ditunggu blog berikutnya kak
BalasHapus